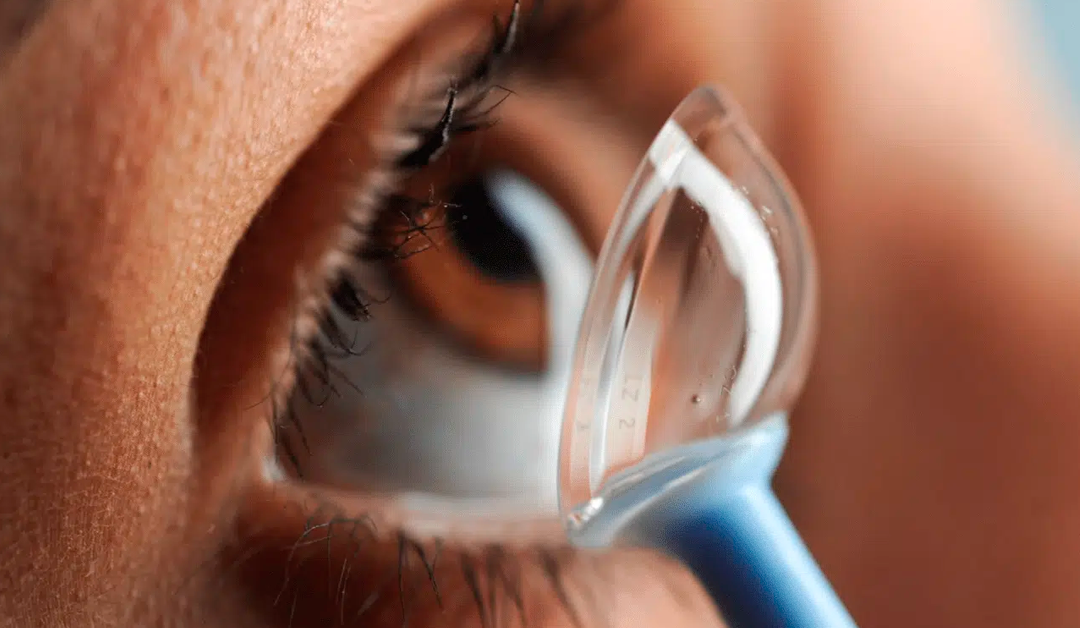
Los lentes de contacto esclerales (LCE) son una alternativa eficaz en el manejo de irregularidades corneales, especialmente en pacientes con queratocono avanzado y casos complejos. Estos lentes, al apoyarse completamente sobre la esclera, o, más específicamente, sobre la conjuntiva bulbar que cubre la esclera, mantienen un espacio de separación con la córnea, denominado bóveda, que promueve una superficie óptica regular, restableciendo la función visual del paciente. Otra ventaja de estos lentes es que reducen al máximo la necesidad de procedimientos invasivos como la queratoplastia. (1–3)
En la correcta forma de inserción del lente, se recomienda llenar la cavidad que forma la superficie cóncava con solución salina libre de preservantes, creando un reservorio de fluido entre el lente y la superficie ocular. Este reservorio cumple una función óptica esencial. Sin embargo, es preciso aclarar que, en este reservorio, existe una limitada dinámica de intercambio lagrimal que favorece la acumulación de partículas, células epiteliales descamadas, lípidos y mediadores inflamatorios, lo que conduce a pérdida de transparencia conocida como turbidez del fluido postlente. (1,4)
El anterior fenómeno se asocia clínicamente con el denominado midday fogging (MDF, por su sigla en inglés), caracterizado por visión borrosa progresiva y molestias durante el día, generalmente al mediodía que obligan al paciente a retirar y reinsertar el lente, afectando la comodidad y la adherencia al uso. Se ha descrito que existen diversos factores que contribuyen a la turbidez del reservorio, incluyendo adaptación inadecuada del lente, clearance excesivo, alineación deficiente de las hápticas y condiciones inflamatorias de la superficie ocular.(1,5)
En este sentido, aunque se han propuesto estrategias para mitigar el MDF, como el uso de soluciones que imitan la composición de la lágrima o la adición de lubricantes oculares, la evidencia clínica sobre su efectividad es limitada. En este contexto, el empleo de soluciones con alta viscosidad y propiedades antiinflamatorias, como el hialuronato de sodio, surge como una alternativa prometedora para mejorar la calidad visual y reducir la turbidez sin comprometer la estabilidad del lente. (1)
Con base en esta problemática, Vurgun y colaboradores (2025), realizan un estudio con el fin de evaluar el impacto del uso de una solución de hialuronato de sodio en el reservorio de lentes esclerales sobre la turbidez del fluido postlente, la estabilidad visual y el asentamiento del lente en pacientes con queratocono, comparándolo con la solución salina convencional. (1)
En la metodología del estudio, se incluyeron 22 pacientes con diagnóstico confirmado de queratocono, cada participante fue adaptado con un LCE de 15 mm de diámetro. El diseño del estudio contempló la comparación intraindividual; esto quiere decir, en el primer día, el lente insertado en el ojo derecho se llenó con solución de hialuronato de sodio al 0,15% libre de preservantes, mientras que en otro día el lente del ojo izquierdo se llenó con solución salina libre de preservantes. (1)
Cabe resaltar que el protocolo de adaptación del lente cumple con las características de: no contacto corneal o limbar, ausencia de compresión vascular y un clearance central entre 200 y 400 μm. Las mediciones incluyeron agudeza visual de alto contraste y bajo contraste antes y después de la adaptación, registradas a las 0, 4 y 8 horas de uso. La turbidez del reservorio postlente se evaluó mediante dos métodos: densidad óptica calculada con tomografía Scheimpflug y una escala de 0 a 4 basada en imágenes OCT de segmento anterior (AS-OCT, por su sigla en inglés). El área central del reservorio de 4 mm se delimitó manualmente para el cálculo automático de densidad promedio. Asimismo, se midió el clearance corneal central y el grado de asentamiento del lente en los mismos intervalos de tiempo. (1) Ver Figura 1.

Figura 1. SA-OCT que muestra el grado de la turbidez del fluido postlente
Entre los resultados principales, se observó que, tras la adaptación de los LCE y un periodo de asentamiento de 30 minutos, la agudeza visual (AV) de alto contraste mejoró significativamente respecto al valor basal con corrección en gafas, en ambos ojos. De forma alterna, la AV de bajo contraste con el test Pelli‑Robson mostró un incremento inmediato hasta aproximadamente 1,23–1,24 unidades LogMAR. En el seguimiento a 0, 4 y 8 horas de uso del LCE, la AV de alto contraste se mantuvo estable sin diferencias significativas, mientras que la AV de bajo contraste presentó un comportamiento diferencial según la solución de relleno del reservorio.(1)
En detalle, en los ojos con hialuronato de sodio se mantuvo estable durante las 8 horas, en tanto que en los ojos con solución salina disminuyó de manera significativa a las 4 y 8 horas respecto al momento inicial. La turbidez del fluido postlente aumentó progresivamente en ambos grupos, evidenciada por el incremento de la densidad óptica medida con tomografía Scheimpflug y por el ascenso de la puntuación en la escala de niebla o neblina o turbidez basada en imágenes de AS‑OCT. Sin embargo, no se observaron diferencias entre soluciones en ninguno de los tiempos evaluados. (1)
En cuanto al clearance corneal central basal, este se situó en el rango previsto para una adaptación óptima (≈300–320 μm), y el asentamiento total del LCE transcurrió con una cinética similar en ambos grupos con alrededor del 70 al 74% del asentamiento durante las primeras 4 horas, sin diferencias en la tasa ni en la magnitud entre hialuronato y solución salina.(1)
Con base en estos resultados, los autores sugieren que el uso de una solución de hialuronato de sodio de mayor viscosidad como fluido de relleno del reservorio no modifica la trayectoria de la turbidez postlente ni acelera el asentamiento del LCE, pero, en cambio, sí se asocia a una mejor preservación de la calidad visual medida como AV de bajo contraste a lo largo de la jornada.
Los autores sugieren que este resultado es clínicamente relevante en el contexto del midday fogging, en el cual, semiológicamente existe un deterioro visual progresivo que a menudo obliga a retirar y reinsertar el lente, con el subsecuente impacto en la adherencia al uso del lente de contacto y la satisfacción del usuario a largo plazo. La estabilidad del bajo contraste con hialuronato podría explicarse por varios mecanismos complementarios, a saber: en primer lugar, su mayor viscosidad favorecería una película líquida más uniforme y estable en el reservorio, lo que reduce microfluctuaciones ópticas y dispersión de la luz, las cuales son muy sensibles en pruebas de contraste.(1)
En segunda instancia, sus propiedades lubricantes y protectoras del epitelio contribuirían a minimizar el desprendimiento celular y la interacción mecánica en la interfase cornea‑reservorio; y, finalmente, su actividad antiinflamatoria podría atenuar el reclutamiento de leucocitos y la liberación de mediadores en el fluido postlente, todos factores implicados en la pérdida de transparencia. Pero, en contraste, los autores aclaran que el ascenso paralelo de la densidad óptica y de la puntuación de turbidez en ambos grupos indica que la acumulación de partículas en un sistema con intercambio lagrimal muy limitado es un fenómeno que ocurre independientemente de la solución empleada. (1)
En estos términos, se sugiere que el hialuronato no impide que la turbidez progrese, pero sí amortigua su consecuencia funcional sobre la sensibilidad al contraste. otro aspecto clave es la dinámica de asentamiento. En este estudio, los autores observaron que, con el LCE, la mayor parte del asentamiento tuvo lugar antes de las 4 horas y fue equivalente para hialuronato y solución salina, lo que sugiere que la viscosidad del reservorio no altera de manera significativa la mecánica de apoyo escleral ni la redistribución de cargas sobre la conjuntiva.
En la práctica clínica, esta observación indica que el utilizar hialuronato en el reservorio no parece comprometer el parámetro crítico del clearance ni exige re‑optimización de la adaptación por cambios de asentamiento. Sin embargo, se debe tener especial cuidado ya que, en este estudio, los autores en su muestra seleccionaron pacientes sin enfermedad de superficie ocular; por lo tanto, no se puede extrapolar el estudio a esta población radicalmente; sobre todo en humanos con disfunción de glándulas de Meibomio (DGM), ojo seco evaporativo o rosácea ocular, en quienes la composición lipídica y celular de la lágrima difiere y el MDF suele ser más manifiesto. (1)
Con todo lo anterior, el uso de hialuronato de sodio libre de preservantes como solución de relleno del reservorio emerge como una estrategia segura que no altera el asentamiento, se describe como compatible al no incrementar la turbidez respecto a la solución salina y es un beneficio el mantener la sensibilidad al contraste durante el día. Esto puede traducirse en menos necesidad de retirar y rellenar el lente por empañamiento, mejor experiencia de uso y mayor adherencia. No obstante, el control del MDF exige un enfoque multimodal consistente en la optimización del clearance central y alineación háptica, manejo de la DGM y lípidos de la película lagrimal, y educación del paciente sobre rutinas de higiene y recambio del reservorio cuando los síntomas lo requieran.(1)
Con lo anterior, los autores concluyen que, en pacientes con queratocono, el uso de hialuronato de sodio de alta viscosidad como solución de reservorio en LCE preserva la agudeza visual de bajo contraste respecto a la solución salina a lo largo de 8 horas de uso continuo, sin aumentar la turbidez postlente ni modificar la tasa o magnitud de asentamiento del LCE.(1)
Adicionalmente, dado su perfil lubricante y reparador epitelial, el hialuronato se posiciona como alternativa preferible para usuarios con susceptibilidad al MDF. La turbidez del reservorio, de todas maneras, progresa en el tiempo con independencia de la solución, lo que resalta la necesidad de estrategias complementarias centradas en la adaptación del LCE y en el manejo de la superficie ocular.(1)
Los autores finalmente recomiendan que se deben realizar futuras investigaciones con periodos de uso más prolongados, inclusión de usuarios habituales de LCE y análisis integrados de depósitos, intercambio lagrimal e inflamación, para delimitar mejor subgrupos, y determinar el efecto del hialuronato en estos casos especiales y además, frecuentes.(1)
Referencias
1. Vurgun EB, Ozkan G, Turhan SA, Toker AE. The Effect of Scleral Lens Reservoir Solution
on Post-lens Fluid Turbidity and Settling in Patients With Keratoconus. Eye Contact Lens. el 1 de
diciembre de 2025;51(12):529–35.
2. Scanzera AC, Deeley M, Joslin C, McMahon TT, Shorter E. Contact Lens Prescribing Trends
for Keratoconus at an Academic Medical Center: Increased Utilization of Scleral Lenses for Severe
Disease. En: Eye and Contact Lens. Lippincott Williams and Wilkins; 2022. p. 58–62.
3. Zhou Y, Lin G, Yu X, Cao Y, Cheng H, Shi C, et al. Deep learning segmentation of the tear fluid reservoir under the sclera lens in optical coherence tomography images. Biomed Opt Express. el 1 de mayo de 2023;14(5):1848.
4. Tse V, Tan B, Kim YH, Zhou Y, Lin MC. Tear dynamics under scleral lenses. Contact Lens and Anterior Eye. el 1 de febrero de 2019;42(1):43–8.
5. Tan B, Zhou Y, Yuen TL, Lin K, Michaud L, Lin MC. Effects of Scleral-lens Tear Clearance on Corneal Edema and Post-lens Tear Dynamics: A Pilot Study. Optometry and Vision Science. el 1 de junio de 2018;95(6):481–90.